Contenido
- Cáncer de mama hereditario
- Mutaciones de genes no BRCA
- Cáncer de mama y pruebas genéticas
- Apoyo para el cáncer de mama hereditario
Además de las mutaciones de los genes BRCA1 y BRCA2, algunas de ellas incluyen mutaciones en ATM, PALB2, PTEN, CDH1, CHEK2, TP53, STK11, PMS2 y más. Veamos qué tan importantes son estas mutaciones no BRCA1 / BRCA2 en el cáncer de mama familiar y algunas de las características de las que se encuentran más comúnmente.
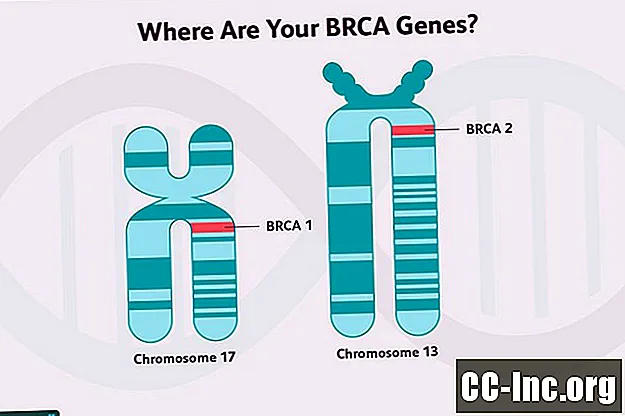
Cáncer de mama hereditario
Actualmente se piensa que entre el 5 y el 10 por ciento de los cánceres de mama son genéticos o familiares (aunque este número puede cambiar a medida que aprendemos más), pero no todos estos cánceres se deben a mutaciones BRCA.
A lo sumo, el 29 por ciento (y probablemente muchos menos) de los cánceres de mama hereditarios dan positivo a las mutaciones de los genes BRCA1 o BRCA2, y muchas personas están realizando pruebas para detectar los otros cambios genéticos conocidos.
Dado que la ciencia detrás del cáncer hereditario provoca mucha ansiedad, por no hablar de confusa e incompleta, es útil comenzar hablando sobre la biología de las mutaciones genéticas y cómo estos cambios en el ADN juegan un papel en el desarrollo del cáncer.
Mutaciones genéticas heredadas frente a adquiridas
Cuando se habla de mutaciones, es importante distinguir entre mutaciones genéticas heredadas y adquiridas.
Las mutaciones genéticas adquiridas o somáticas han recibido mucha atención en los últimos años, ya que estas mutaciones provocan cambios que impulsan el crecimiento del cáncer. Las terapias dirigidas, fármacos que se dirigen a vías específicas relacionadas con estos cambios, han mejorado significativamente el tratamiento de algunos cánceres como el de pulmón.
Sin embargo, las mutaciones adquiridas no están presentes desde el nacimiento, sino que se forman en cualquier momento después del nacimiento en el proceso de que una célula se convierta en una célula cancerosa. Estas mutaciones afectan solo a algunas células del cuerpo. No se heredan de uno de los padres, sino que se "adquieren" cuando el ADN de las células está expuesto al daño del medio ambiente o como resultado de los procesos metabólicos normales del cuerpo.
Las mutaciones heredadas o de la línea germinal, por el contrario, son cambios genéticos con los que las personas nacen y que se transmiten de uno o ambos padres. Estas mutaciones afectan a todas las células del cuerpo. Son estas mutaciones heredadas (y otros cambios genéticos) las que pueden aumentar la probabilidad de que una persona desarrolle cáncer y explican lo que se conoce como cáncer de mama hereditario o familiar.
Mutaciones genéticas hereditarias (línea germinal) frente a mutaciones genéticas adquiridas (somáticas)¿Cómo aumentan el riesgo de cáncer las mutaciones genéticas hereditarias?
Muchas personas se preguntan cómo exactamente un gen anormal o una combinación de genes pueden conducir al cáncer de mama, y una breve discusión sobre la biología es útil para comprender muchas de las preguntas, como por qué no todas las personas que tienen estas mutaciones desarrollan cáncer.
Nuestro ADN es un modelo o código que se utiliza para fabricar proteínas. Cuando el mapa o el código es incorrecto (como las "letras" en un gen en particular), da las direcciones incorrectas para sintetizar una proteína. Entonces, la proteína anormal no puede realizar su trabajo habitual. No todas las mutaciones genéticas aumentan el riesgo de cáncer y, de hecho, la mayoría no lo hace. Las mutaciones en los genes responsables del crecimiento y la división de las células, o "mutaciones impulsoras", son las que impulsan el crecimiento de los cánceres. Hay dos tipos principales de genes que, cuando mutan, pueden conducir a un crecimiento descontrolado conocido como cáncer: los oncogenes y los genes supresores de tumores.
Varios de los genes asociados con un mayor riesgo de cáncer de mama son genes supresores de tumores. Estos genes codifican proteínas que funcionan para reparar el daño al ADN en las células (daño por toxinas en el medio ambiente o los procesos metabólicos normales en las células), sirven para eliminar células que no se pueden reparar o regular el crecimiento de otras formas. Los genes BRCA1 y BRCA2 son genes supresores de tumores.
Muchos de estos genes son autosómicos recesivos, lo que significa que cada persona hereda una copia del gen de cada padre y ambas copias deben estar mutadas para aumentar el riesgo de cáncer. De manera simplista, esto significa que una combinación de factores genéticos y ambientales (una mutación adquirida en el otro gen) debe actuar en conjunto para provocar el desarrollo del cáncer. Sumado a esto, por lo general, deben ocurrir varias mutaciones para que una célula se convierta en una célula cancerosa.
Qué significa tener una predisposición genética al cáncerPenetrancia genética
No todas las mutaciones o cambios genéticos aumentan el riesgo de cáncer de mama en el mismo grado, y este es un concepto importante para cualquiera que esté considerando las pruebas genéticas, especialmente porque muchas personas han oído hablar del riesgo muy alto conferido por las mutaciones BRCA. La penetrancia genética se define como la proporción de personas con una mutación que experimentarán la afección (en este caso, desarrollarán cáncer de mama).
Para algunas mutaciones, el riesgo de cáncer de mama es muy alto. Para otros, el riesgo puede incrementarse solo en un factor de 1,5. Es importante comprender esto cuando se habla de posibles opciones preventivas.
Epigenética
Otro concepto importante que es importante para comprender la genética y el cáncer, aunque demasiado complejo para explorarlo en detalle aquí, es el de la epigenética. Hemos aprendido que los cambios en el ADN que no involucran cambios en los pares de bases (nucleótidos) o las "letras" que codifican una proteína, pueden ser igualmente importantes en el desarrollo del cáncer. En otras palabras, en lugar de cambios estructurales en la columna vertebral del ADN, puede haber cambios moleculares que cambien la forma en que se lee o se expresa el mensaje.
Mutaciones de genes no BRCA
Las mutaciones del gen BRCA son la anomalía genética más conocida asociada con el cáncer de mama, pero está claro que hay mujeres que están predispuestas al cáncer de mama según sus antecedentes familiares, que dan negativo en las pruebas.
Un estudio de 2017 encontró que las mutaciones BRCA representaron solo del 9 al 29 por ciento de los cánceres de mama hereditarios. Sin embargo, incluso cuando se realizaron pruebas para otras 20 a 40 mutaciones conocidas, solo entre el 4 y el 11 por ciento de las mujeres dieron positivo. En otras palabras, del 64 al 86 por ciento de las mujeres sospechosas de tener cáncer de mama hereditario dieron negativo en las pruebas de mutaciones BRCA y de 20 a 40 más.
Cáncer de mama familiar no BRCA1 / BRCA2
Nuestro conocimiento sobre las mutaciones genéticas que aumentan el riesgo de cáncer de mama aún es incompleto, pero ahora sabemos que existen al menos 72 mutaciones genéticas relacionadas con el cáncer de mama hereditario. Se cree que estas mutaciones (y otras aún no descubiertas) son responsables del 70% al 90% de los cánceres de mama hereditarios que dan negativo en las pruebas de mutaciones del gen BRCA. El acrónimo BRCAX se ha acuñado para describir estas otras mutaciones, que significa no BRCA1 Cáncer de mama familiar relacionado con BRCA2.
72 mutaciones genéticas vinculadas al cáncer de mama hereditarioLas anomalías genéticas a continuación difieren en su frecuencia, la cantidad de riesgo asociado, el tipo de cáncer de mama con el que están vinculados y otros cánceres asociados con las mutaciones.
La mayoría de estos cánceres de mama son similares en características (como el tipo de cáncer, el estado de los receptores de estrógeno y el estado de HER2) a los cánceres de mama esporádicos o no hereditarios, pero hay excepciones. Por ejemplo, algunas mutaciones están más fuertemente asociadas con el cáncer de mama triple negativo, incluidas las mutaciones en BARD1, BRCA1, BRCA2, PALB2yRAD51D.
Variabilidad dentro de las mutaciones
No todas las personas que tienen las siguientes mutaciones genéticas son iguales. En general, puede haber cientos de formas en las que estos genes mutan. En algunos casos, el gen producirá proteínas que suprimen el crecimiento del tumor, pero las proteínas no funcionarán tan bien como la proteína normal. Con otras mutaciones, es posible que la proteína no se produzca en absoluto.
BRCA (una breve reseña para comparar)
Las mutaciones del gen BRCA 1 y las mutaciones del gen BRCA2 están asociadas con un mayor riesgo de desarrollar cáncer de mama, así como con algunos otros cánceres, aunque los dos difieren algo en ese riesgo.
En promedio, el 72 por ciento de las mujeres que tienen mutaciones BRCA1 y el 69 por ciento que tienen genes BRCA2 mutados desarrollarán cáncer de mama a la edad de 80 años.
Además, los cánceres de mama asociados con estas mutaciones pueden diferir. Los cánceres de mama en mujeres que tienen mutaciones BRCA1 tienen más probabilidades de ser triple negativo. Alrededor del 75 por ciento son receptores de estrógeno negativos y también tienen menos probabilidades de ser HER2 positivo. También es más probable que tengan un grado tumoral más alto. Los cánceres de mama en mujeres con mutaciones BRCA2, por el contrario, son similares a los cánceres en mujeres que no son portadoras de mutaciones del gen BRCA.
Gen ATM (ATM serina / treonina quinasa)
El gen ATM codifica proteínas que ayudan a controlar la tasa de crecimiento de las células. También ayudan en la reparación de células dañadas (células que han sufrido daño en el ADN por toxinas) activando enzimas que reparan este daño.
Aquellos que tienen dos copias del gen mutado tienen un síndrome autosómico recesivo poco común conocido como ataxia-telangiectasia. Con la ataxia-telangiectasia, las proteínas defectuosas no solo aumentan el riesgo de cáncer, sino que también hacen que algunas células del cerebro mueran demasiado pronto, lo que resulta en un trastorno neurodegenerativo progresivo.
Las personas que tienen solo una copia mutada del gen (aproximadamente el 1 por ciento de la población) tienen un riesgo de por vida del 20 al 60 por ciento de desarrollar cáncer de mama.
Se cree que las personas que tienen esta mutación están predispuestas al cáncer de mama a una edad temprana, así como a desarrollar cáncer de mama bilateral.
Se recomienda la detección del cáncer de mama con resonancias magnéticas de mama a partir de los 40 años, y es posible que las mujeres deseen considerar las mastectomías preventivas. Las personas con un gen ATM mutado también parecen estar predispuestas a los cánceres de tiroides y páncreas y son más sensibles a la radiación.
PALB2
Las mutaciones en el gen PALB2 también son una causa importante de cáncer de mama hereditario. El gen PALB2 codifica una proteína que trabaja junto con la proteína BRCA2 para reparar el ADN dañado en las células. En general, el riesgo de por vida de cáncer de mama con una mutación PALB2 es de hasta un 58 por ciento, aunque esto puede variar según la edad. El riesgo es de 8 a 9 veces el promedio para las mujeres menores de 40 años, pero alrededor de 5 veces el promedio para las mujeres mayores de 60 años.
Entre los que portan una copia del gen, el 14 por ciento desarrollará cáncer de mama a los 50 años y el 35 por ciento a los 70 años (menos que con las mutaciones BRCA).
Las personas que tienen una mutación PALB2 y desarrollan cáncer de mama pueden tener un mayor riesgo de morir a causa de la enfermedad.
Las personas que heredan 2 copias del gen PALB2 mutado tienen un tipo de anemia de Fanconi caracterizada por recuentos muy bajos de glóbulos rojos, glóbulos blancos y plaquetas.
CHEK2
El gen CHEK2 codifica una proteína que se activa cuando se daña el ADN. También activa otros genes implicados en la reparación celular.
Los riesgos de por vida para los portadores de mutaciones que truncan CHEK2 son 20 por ciento para una mujer sin pariente afectado, 28 por ciento para una mujer con un pariente de segundo grado afectado, 34 por ciento para una mujer con un pariente de primer grado afectado y 44 por ciento para una mujer con un pariente de primer y segundo grado afectado.
Tanto para hombres como para mujeres, el gen también aumenta el riesgo de cáncer de colon y linfoma no Hodgkin.
CDH1
Las mutaciones en CDH1 causan una afección conocida como síndrome de cáncer gástrico hereditario.
Las personas que heredan este gen tienen un riesgo de por vida de hasta un 80 por ciento de desarrollar cáncer de estómago y hasta un 52 por ciento de desarrollar cáncer de mama lobular.
El gen codifica una proteína (cadherina epitelial) que ayuda a que las células se adhieran entre sí (una de las diferencias entre las células cancerosas y las células normales es que las células cancerosas carecen de estos químicos de adhesión que las hacen adherirse). Los cánceres en las personas que heredan esta mutación tienen más probabilidades de hacer metástasis.
PTEN
Las mutaciones en el gen PTEN son una de las mutaciones del gen supresor de tumores más comunes. El gen codifica proteínas que regulan el crecimiento de las células y también ayuda a que las células se unan.
Las mutaciones en el gen parecen aumentar el riesgo de que las células cancerosas se desprendan de un tumor y hagan metástasis. PTEN se asocia con un síndrome llamado síndrome de tumor de hamartoma PTEN, así como con el síndrome de Cowden.
Las mujeres que portan una mutación PTEN tienen un riesgo de por vida de desarrollar cáncer de mama hasta en un 85 por ciento, y también tienen un mayor riesgo de cambios benignos en las mamas, como enfermedad fibroquística, adenosis y papilomatosis intraductal.
Las mutaciones también están relacionadas con un mayor riesgo de cáncer de útero (y fibromas uterinos benignos), cáncer de tiroides, cáncer de colon, melanoma y cáncer de próstata.
Los síntomas no relacionados con el cáncer incluyen un tamaño de cabeza grande (macrocefalia) y la tendencia a formar tumores benignos conocidos como hamartomas.
STK11
Las mutaciones en STK11 están asociadas con una condición genética conocida como síndrome de Peutz-Jegher. STK11 es un gen supresor de tumores que participa en el crecimiento celular.
Además de un mayor riesgo de cáncer de mama (con un riesgo de por vida de hasta el 50 por ciento), el síndrome conlleva un mayor riesgo de muchos cánceres, algunos de los cuales incluyen cáncer de colon, cáncer de páncreas, cáncer de estómago, cáncer de ovario, cáncer de pulmón, cáncer de útero y más.
Las afecciones no relacionadas con el cáncer asociadas con la mutación incluyen pólipos no cancerosos en el tracto digestivo y el sistema urinario, pecas en la cara y el interior de la boca, y más. Las pruebas de detección del cáncer de mama a menudo se recomiendan para mujeres que comienzan en los 20 y, a menudo, con resonancia magnética con o sin mamografías.
TP53
El gen TP53 codifica proteínas que detienen el crecimiento de células anormales.
Estas mutaciones son extremadamente comunes en el cáncer, con adquirido Se encuentran mutaciones en el gen p53 en alrededor del 50 por ciento de los cánceres.
Las mutaciones hereditarias son menos comunes y están asociadas con afecciones conocidas como síndrome de Li-Fraumeni o síndrome similar a Li-Fraumeni (que tiene un menor riesgo de cáncer). La mayoría de las personas que heredan la mutación desarrollan cáncer a los 60 años y, además del cáncer de mama, son propensas a desarrollar cáncer de huesos, cáncer suprarrenal, cáncer de páncreas, cáncer de colon, cáncer de hígado, tumores cerebrales, leucemia y más. No es raro que las personas con la mutación desarrollen más de un cáncer primario.
Se cree que las mutaciones hereditarias en el gen p53 representan alrededor del 1 por ciento de los casos de cáncer de mama hereditario. Los cánceres de mama asociados con la mutación suelen ser positivos para HER2 y tienen un grado tumoral alto.
Síndrome de Lynch
El síndrome de Lynch o cáncer colorrectal hereditario sin poliposis se asocia con mutaciones en varios genes diferentes, incluidos PMS2, MLH1, MSH2, MSH6 y EPCAM.
El PMS2, en particular, se ha asociado con el doble de riesgo de cáncer de mama. El gen funciona como un gen supresor de tumores, que codifica una proteína que repara el ADN dañado.
Además del cáncer de mama, estas mutaciones conllevan un alto riesgo de cáncer de colon, ovario, útero, estómago, hígado, vesícula biliar, intestino delgado, riñón y cerebro.
Otras mutaciones
Hay varias otras mutaciones genéticas asociadas con un mayor riesgo de desarrollar cáncer de mama, y se espera que se descubran más en un futuro próximo. Algunos de estos incluyen:
- BRIP1
- BARD1
- MRE11A
- NBN
- RAD50
- RAD51C
- SEC23B
- BLM
- MUTYH
Cáncer de mama y pruebas genéticas
En la actualidad, hay pruebas disponibles para las mutaciones del gen BRCA, así como las mutaciones ATM, CDH1, CHEK2, MRE11A, MSH6, NBN, PALB2, PMS2, PTEN, RAD50, RAD51C, SEC23B y TP53, y se espera que esta área se expanda dramáticamente en un futuro próximo.
Sin embargo, tener estas pruebas disponibles plantea muchas preguntas. Por ejemplo, ¿quién podría tener cáncer de mama hereditario y quién debería hacerse la prueba? ¿Qué debe hacer si da positivo en uno de estos genes?
Idealmente, cualquier prueba debe realizarse solo con la guía y ayuda de un asesor genético. Hay dos razones para esto.
Una es que puede ser devastador saber que es portador de una mutación que puede aumentar su riesgo, y la guía de alguien que esté al tanto del manejo y detección recomendados es invaluable.
Como se señaló anteriormente, algunas mutaciones confieren un alto riesgo y otras un riesgo mucho menor. Algunas mutaciones pueden ser más preocupantes en una etapa temprana de la vida (digamos, a los 20 años), mientras que otras pueden no requerir una detección temprana. Un asesor genético puede ayudarlo a conocer lo que se recomienda actualmente con respecto a la detección de su mutación particular, teniendo en cuenta cualquier otro factor de riesgo que pueda tener.
La otra razón por la que la asesoría genética es tan importante es que puede tener un riesgo significativo de desarrollar cáncer de mama incluso si sus pruebas son negativas. Aún queda mucho por aprender, y un asesor genético puede ayudarlo a analizar su historial familiar para ver si puede tener un alto riesgo a pesar de las pruebas negativas y planificar la detección en consecuencia.
Pruebas genéticas para el cáncer de mamaApoyo para el cáncer de mama hereditario
Así como las personas a las que se les ha diagnosticado cáncer de mama necesitan apoyo, las que portan genes que aumentan el riesgo necesitan apoyo. Afortunadamente, existen organizaciones que se enfocan específicamente en apoyar a las personas en esta situación.
Una organización, FORCE, que es un acrónimo de Enfrentando nuestro riesgo de cáncer empoderado, ofrece una línea de ayuda, un tablero de mensajes e información para quienes enfrentan un cáncer hereditario.
Hay otras organizaciones y comunidades de apoyo disponibles para ayudar a las personas a afrontar las decisiones relacionadas con un diagnóstico de cáncer de mama hereditario.
El término "precursor" fue acuñado por FORCE para describir a las personas que sobreviven a una predisposición al cáncer de mama. Si esta es la situación a la que te enfrentas, no estás solo, y usando el hashtag #previvor, puedes encontrar muchos otros en Twitter y otras redes sociales.
Una palabra de Verywell
Puede ser abrumador conocer las muchas mutaciones genéticas diferentes que aumentan el riesgo de cáncer de mama más allá de las mutaciones BRCA, pero estas "otras" mutaciones son de gran importancia sabiendo que las mutaciones BRCA representan una minoría relativa de cánceres de mama familiares. Al mismo tiempo, la ciencia que analiza el cáncer de mama hereditario está todavía en su infancia y hay mucho que aprender. Si le preocupa que pueda tener una mutación o ha aprendido que la tiene, es útil aprender todo lo que pueda. Las organizaciones de cáncer hereditario, como FORCE, no solo pueden brindarle más información, sino que también pueden ayudarlo a conectarse con otras personas que enfrentan un viaje con preguntas e inquietudes similares.